太好了!阿尔茨海默病(Alzheimer's Disease)领域最近迎来了久违的好消息~7月6日,美国FDA完全批准了卫材 /百健开发的阿尔茨海默病治疗药物仑卡奈单抗(lecanemab)。这是20年来首款获得FDA完全批准的阿尔茨海默病新药。
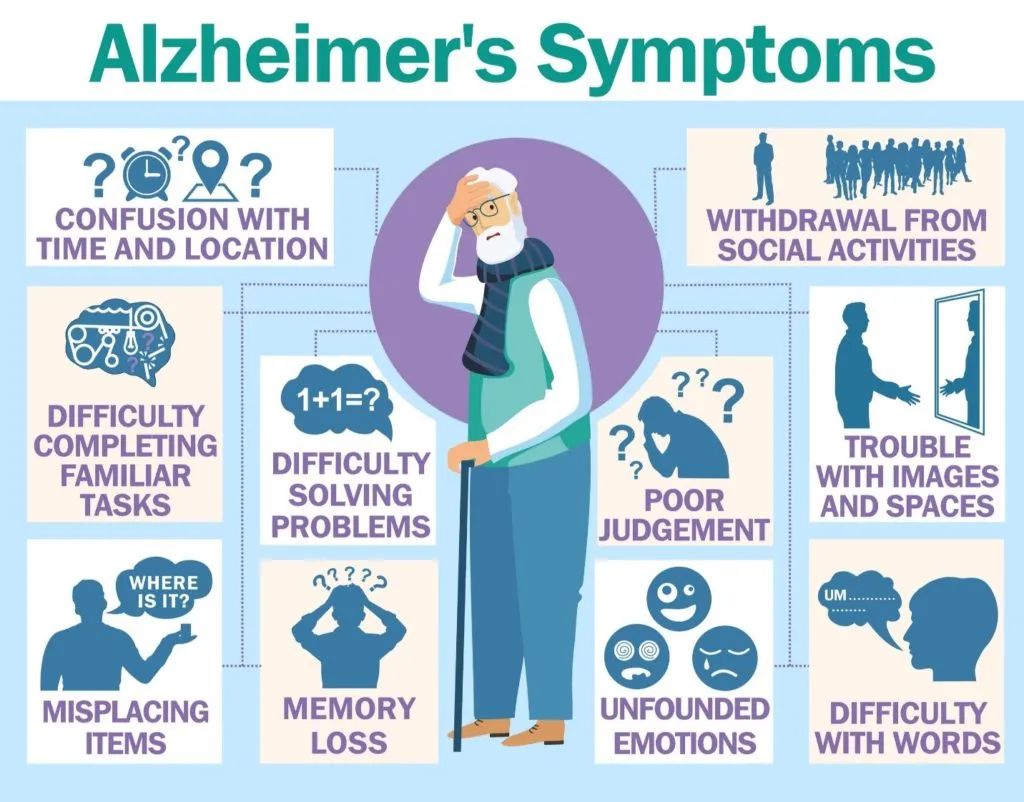
仑卡奈单抗目前会在美国上市,并提供给美国600万阿尔茨海默病患者中的大多数人。阿尔茨海默症又称老年痴呆症,是老年人的健康劲敌。对于经历了太多次失败的阿尔茨海默症领域,这样的成功实在是来之不易,值得被载入史册!阿尔茨海默病的患者众多,但可用的治疗药物却寥寥无几。阿尔兹海默病是老年期痴呆最主要的类型,表现为记忆减退、词不达意、思维混乱、判断力下降等脑功能异常和性格行为改变等。一般在65岁以前发病为早发型,65岁以后发病为晚发型。
目前普遍认为,阿尔兹海默病的病因是由β-淀粉样蛋白(Aβ)和Tau淀粉样蛋白沉积导致神经元病变。Aβ阳性是阿尔兹海默病确诊的核心依据。据世界卫生组织报告,全球约有5000万人患有痴呆症,其中阿尔茨海默病是最常见的类型,可能占痴呆症病例的60%至70%。
但另一方面,由于阿尔茨海默病的发病机制复杂,之前仅有几种药物(如多奈哌齐、利斯的明、加兰他敏、美金刚)获得FDA和世界主要国家的批准并使用。这些药物虽然可以在一定程度上改善患者认知症状,但并不能延缓病程的进展。
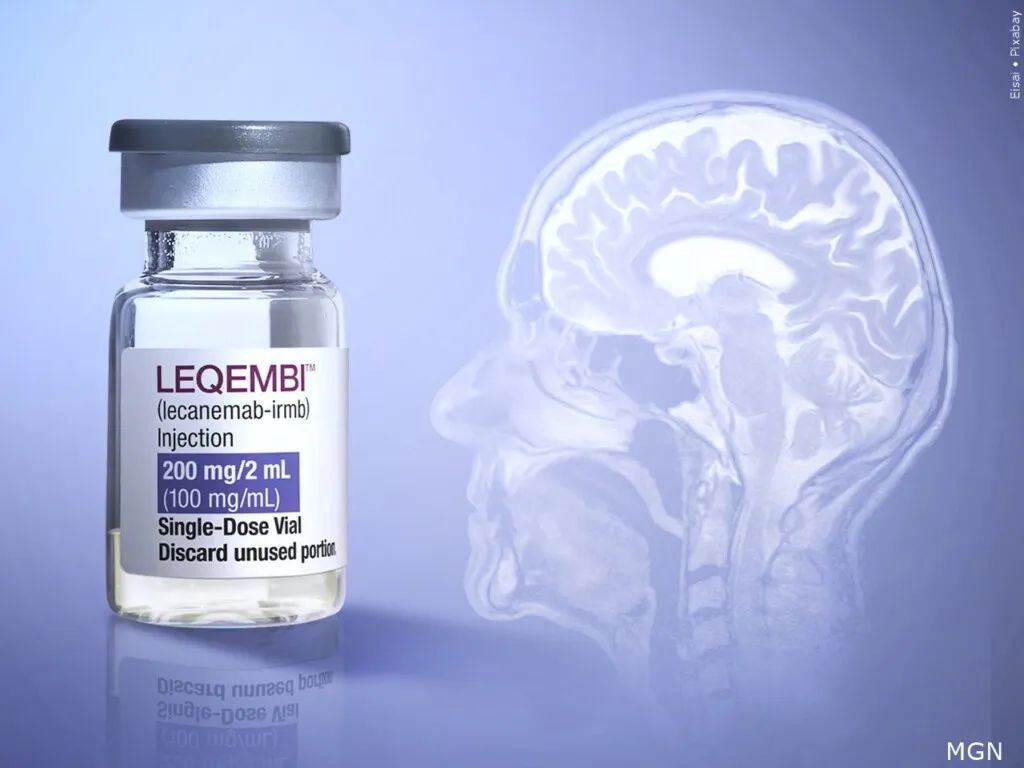
最新研发并上市的仑卡奈单抗,是一种人源化免疫球蛋白G1单克隆抗体,能够通过与可溶性Aβ聚合体结合,并且促进它们的清除,从而具有改变AD病理,缓解疾病进展的潜力。
仑卡奈单抗的获批,对于阿尔茨海默病药物研发领域而言,具有里程碑式的意义。仑卡奈单抗由日本卫材株式会社与瑞士公司BioArctic合作研发,又与美国生物科技公司渤健共同负责该产品用于阿尔茨海默病治疗的开发与商业化。2023年1月,获得FDA加速批准上市。作为加速批准的上市后要求,FDA要求申请人进行临床试验(通常称为验证性研究),以验证仑卡奈单抗的预期临床益处。试验结果显示,仑卡奈单抗展示了积极的治疗效果。
6月9日,FDA外周和中枢神经系统药物咨询委员会以6:0投票赞成完全批准仑卡奈单抗的决定。这一药物的获批具有里程碑意义,标志着该药物已经通过了所有必要的临床试验,证明其对大多数人群的安全性和有效性,可被广泛用于医疗实践。
“仑卡奈单抗是针对和影响这种疾病过程的最新疗法,而不是只治疗相关症状。”美国FDA药品评价与研究中心(CDER)主任比利·邓恩(Billy Dunn)曾如此评价。据悉,该药物每两周静脉注射一次,根据患者体重剂量为10mg/kg,按照患者体重80kg计算,每人年用量20g,年费用2.65万美元。
同时卫材表示,到2030年,仑卡奈单抗在全球的年销售额将达到70亿美元。阿尔茨海默病领域堪称堪称药物“研发黑洞”,许多大药企在这上面烧了不少钱,却始终未见成效。1906年11月3日,德国医生爱罗斯·阿尔茨海默首次将阿尔茨海默病拉入公众的视野中,此后100多年里,各路学者、企业在阿尔茨海默病药物的研发中投入巨大的时间与金钱,试图找到治疗阿尔茨海默病的最优解。
但迄今为止,像仑卡奈单抗一样的成功者寥寥。在阿尔茨海默病药物赛道上,更多的是失败案例。过去十多年,礼来制药、渤健、罗氏等药企都花费数百亿美元,在阿尔茨海默病药物的研发上前仆后继,但坏消息往往多过好消息。
2018年美国药物生产与研发协会数据显示,2000-2017年,全球累计在阿尔茨海默病药物上的研发投入超过6000亿美元,失败的临床药物超过300种,失败率高达99.6%。另据美国药品研究与制造商协会(PhRMA)的报告数据,从1998-2017年,全球有146款阿尔茨海默病药物进入临床试验“终点”,其中仅4款成功走向市场。
2023年1月,在美国FDA宣布仑卡奈单抗获批后,在美上市的阿尔茨海默病药物也仅仅只有8款而已~
【声明】内容部分及图片来源于(北美湾区天天汇),本文章仅做分享不代表任何观点,如有侵犯您的权益,请先与我们联系,我们会第一时间进行处理。